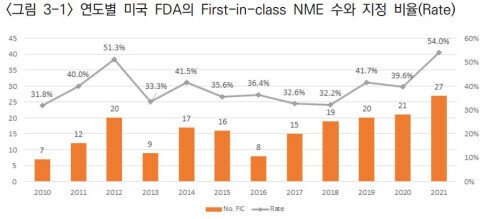
연도별 미국 FDA의 FIC NME 수와 지정 비율(그래프=한국보건산업진흥원 제공)
[메디컬투데이=이한희 기자] 미국 FDA의 혁신신약 시판허가 현황을 분석한 결과 항암제는 비항암제에 비해 혁신신약 지정 비율이 0.40배 낮은 것으로 나타났다.
최근 한국보건산업진흥원은 ‘혁신신약 개발 영향요인’ 보고서를 발표했다.
제약 산업에서 혁신성 연구는 정책적인 측면에서 매우 중요한 논의 대상이다. 혁신의약품은 미충족 의료에 대한 필요가 있는 환자들에게 치료의 기회를 주고 제약기업들에게 매출 증대와 인지도 향상에 긍정적 요인이 된다.
보고서에 따르면 미국 FDA는 혁신신약(Fist-in-class, FIC)을 ‘특정한 의학적 생태를 치료하기 위한 새롭고 독특한 행동 매커니즘을 사용하는 의약품’으로 정의하고 있다.
미국 FDA는 2010년부터 2021년까지 시판허가를 낸 신약(New Molecular Entities, NME)는 482개다. 이 중 FIC로 지정된 약물은 전체의 39.6%인 191개다.
NME 중 FIC 비율은 2010년부터 2012년까지 31.8%에서 51.3%로 증가하다가 2013년부터 2018년까지 33.3%에서 32.2%로 감소 추세에 있었다. 2019년 이후 다시 FIC 지정 비율이 41.7%로 증가했고 2021년에는 54.0%로 기간 내 최대치를 보였다.
482개의 NME 중 항암제는 128개였다. 이 중 가장 많은 적응증은 백혈병(Leukemia)이었으며 21개가 승인됐다. 이 중 9개는 FIC였다.
보고서는 이에 대해 “항암 치료에 사용되는 기존의 약물과 비교해 효능이나 작용 기전에 차이가 있어야 FIC로 분류될 수 있지만 항암제의 경우 FIC 약물이 허가된 이후에도 유사한 기전의 신약들이 허가를 다수 받고 있어서 FIC 지정 비율이 낮을 것으로 보인다”고 설명했다.
실제로 지난 10년 동안 백혈병 치료를 위한 표적항암제(Targeted drugs agent) 개발이 활발했다. 백혈병 치료를 이한 새로운 타겟이나 기전의 치료제가 개발되면서 이들에 대해서는 혁신성이 대부분 인정됐다. 그러나 2020년 이후에 개발된 백혈병 치료제 3건은 모두 FIC에 포함되지 못했다. 이는 혁신성 여부에 있어서 신규성이 요소가 된다는 방증이기도 하다.
FDA가 허가한 NME를 분석한 결과 FIC 지정 확률이 희귀의약품은 비희귀의약품에 비해 약 3.59배, 항체치료제는 약 3.11배 더 높고 항암제는 비항암제에 비해 약 0.40배 낮았다.
국내 신약 파이프라인을 보면 2022년 기준으로 전체 1900건 중 38.1%가 항암제였다.
이에 보고서는 “국내 항암제를 개발하고 있는 제약기업들이 적절하게 글로벌 시장 진출을 하기 위한 전략을 수립할 수 있도록 글로벌 항암 시장에 대한 심층적 분석과 장기 예측 자료를 제공할 수 있는 ‘마켓 인텔리전스(Market Intelligence)'의 지원 강화를 고려해야 한다”고 주장했다.
메디컬투데이 이한희 hnhn0414@mdtoday.co.kr
- * Copyright ⓒ 메디컬투데이 All Rights Reserved.
- * 본 기사의 내용은 메디컬투데이 언론사에서 제공한 기사이며 헬스조선의 편집방향과 일치하지 않을 수도 있습니다.(관련 문의는 해당 언론사에 연락부탁드립니다)
출처 : https://health.chosun.com/news/dailynews_view.jsp?mn_idx=488088
'병원 치료 > 항암' 카테고리의 다른 글
| 美 항암신약 가속승인 기준 강화...'RCT 연구 강조' (0) | 2023.04.09 |
|---|---|
| 요로상피암, 초기옵션 다양해진다 (0) | 2023.04.09 |
| 新 면역항암제 등장 '자이니즈', 메르켈 세포암 경쟁 (0) | 2023.04.01 |
| 암세포 엑소좀 파괴하는 면역치료제 신물질 발굴 (0) | 2023.03.31 |
| 항암제 거래 73%가 전임상 단계 (0) | 2023.03.29 |



